제넥신의 혁신 신약인 자궁경부전암 치료제 (GX-188E)가 식품의약품안전처로부터 3월 11일 임상2상 승인을 받았다. 금번 임상 2상 시험은 제일병원, 서울 성모병원, 고려대 구로병원, 대구 동산병원 등 총 4개 기관에서 72명의 환자들을 대상으로 진행될 예정이며, 2015년 상반기에는 최종 임상 결과의 확인이 가능할 전망이다.
전세계 여성암 2위인 자궁경부암은 인유두종 바이러스(human papilloma virus; HPV)의 장기간에 걸친 감염에 의해 발생한 자궁경부전암이 계속적으로 진행이 되어 발병하는 암이다. 기존의 예방백신은 이미 바이러스에 감염된 환자들에게는 효과가 없어서, 자궁경부 감염 부위를 제거하는 수술만이 유일한 치료법이지만, 수술을 할 경우 불임, 유산, 미숙아 출산 등의 부작용 및 재발 가능성이 있어서, 안전하고 근본적인 치료제가 필요한 상황이다.
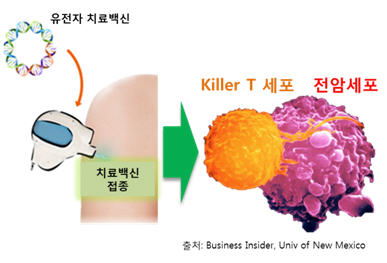
GX-188E는 첨단 면역학적 기술 기반의 유전자 치료제로서 환자에게 killer T 세포 면역반응을 유도하여 바이러스에 의해서 변형된 전암세포를 선택적으로 제거함으로써 질병을 완치시킬 수 있는 혁신 신약으로 자궁경부전암 외에도 외음부상피내종양, 항문상피내종양, 두경부암 등 다수의 적응증으로 확대가 가능하다.
보건복지부의 보건의료연구개발사업 지원 하에 국내 자궁경부전암 환자들을 대상으로 한 임상 1상 시험에서 GX-188E의 안전성 및 면역원성이 확인되었으며, 높은 비율로 수술 없이 질환을 치료하는 결과가 나타나 후속 임상2상을 곧바로 진행하게 되었다. 국내 임상 2상에 이어 미국, 유럽 중심의 해외 임상 2상도 진행 예정이며, 글로벌 기업과의 협력을 적극 추진하여 글로벌 사업화 및 세계 최초의 자궁경부전암 치료백신 출시를 목표로 임상 개발을 가속화 할 계획이다.
뉴스타운
뉴스타운TV 구독 및 시청료 후원하기
뉴스타운TV
























![[단독] 북한산 인수봉, 구조 헬기 긴급 출동 장면 포착!](/news/photo/202511/669971_628773_447.jpg)






