셀리버리는 내재면역제어 면역염증치료신약 iCP-NI의 코로나19 치료제로써 임상개발 상황에서, iCP-NI에 관심을 보이는 복수의 글로벌 제약사들과 기술이전 (Licensing-Out) 및 권역별 판권협상 (Regional Partnership)을 진행중이라고 밝혔다.
(주)셀리버리는 바이오-유럽 (Bio-Europe), JP 모건 헬스케어 컨퍼런스 (J.P. Morgan Healthcare Conference) 및 바이오-인터내셔널 (Bio International Convention)등 글로벌 파트너링 컨퍼런스를 통해 현재 코로나19 치료적응증을 포함한 5개 염증성질환 적응증 치료제 [코로나19 주사제, 패혈증 주사제, 아토피피부염 주사제, 코로나19 흡입제 및 급성호흡곤란증후군 흡입제]로 개발중인 iCP-NI에 지대한 관심있는 글로벌 바이오제약社들과 사업化에 대한 긴밀한 논의를 지속해 왔으며, 임상개발이 가시화됨에 따라 본격적인 라이센싱 및 지역판권 협상을 하고있다.
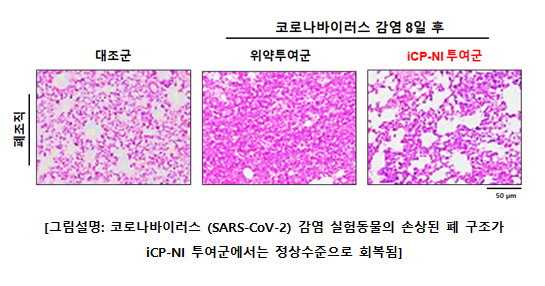
iCP-NI는 각종 병원성 세균 및 바이러스 감염으로 촉발되는 면역폭풍이라 일컬어지는 싸이토카인-스톰 (Cytokine Storm)을 제어하는 면역치료제로써, 염증으로 인한 비가역적인 장기손상 및 중증화에 따른 치명율을 제어할 수 있는 바이오신약이다. 셀리버리는 iCP-NI를 감염병 (Infectious Disease) 치료제로 우선적으로 개발 중에 있는데, 특히 코로나바이러스 (SARS-CoV-2) 감염으로 인해 발병하는 코로나19 (COVID-19)의 핵심증상인 싸이토카인-스톰 및 폐기관지 조직파괴를 동반한 중증환자의 경우, 폐 손상으로 인한 급성호흡곤란증후군 (Acute Respiratory Distress Syndrome: ARDS) 등을 보이면서 다른 장기도 손상되어 사망에까지 이르게 한다. 이런 강력한 감염병에 대해 iCP-NI는 면역세포의 이동과 활성, 싸이토카인의 생성기전을 저해하여 염증을 완화하고, 감염환자의 생존율을 증가시킬 수 있는 바이오신약으로써 큰 기대를 받고있다.
현재 팬데믹 상황인 감염병 코로나19 뿐만 아니라, 염증이 주요 원인이 되는 다양한 염증성질환들에 대해서도 개발이 확장되어 진행되고 있다. 대표적인 급성염증증상인 패혈증 (Sepsis) 및 아토피피부염 (Atopic Dermatitis)에 대한 주사치료제 (IV)는 현재 진행되고 있는 코로나19에 대한 임상1상 개발이 끝나는대로, 임상1상 반복없이 바로 임상2상에 돌입한다는 계획이다. 또한, 주사제가 아닌 환자 친화적 제형으로서 흡입제형 (Inhalation)의 개발이 이루어지고 있다. 이는 역시 코로나19를 포함하는 지역사회감염 폐렴 (Community Acquired Pneumonia: CAP)를 대상으로 한 임상1상 이후, 급성호흡곤란증후군 (ARDS)에 대해 역시 임상1상 반복없이 바로 임상2상에 진입하는 임상개발계획이 진행중이라고 개발 담당자는 밝혔다. 이로써, 셀리버리는 2022년 말까지 2개 제형의 5개 적응증 치료제에 대해 임상단계 개발 (Clinical-Stage Development)을 하는 전혀 다른 차원의 바이오 제약사로 발돋움한다는 계획이다.
셀리버리 임상개발 책임자는, “그간 순탄치 않았으나 임상진입을 앞두고 있는 현 상황에서 iCP-NI에 대한 글로벌 기업들의 사업化 문의 및 협업 요청에 부응하여 본격적인 논의를 진행중이다. 코로나19 치료제로 유럽기반 글로벌 바이오제약社의 공동개발 제안, 일본 Top10 제약사의 일본 내 지역판권 요청 및 중국 대형바이오제약社의 중국시장을 타겟으로 한 공동개발 요청 등을 포함해서 복수의 제약사들과 사업化를 위한 비즈니스를 논의하고 있는 상황이다. 역량있는 해외 파트너社들과의 라이센싱-아웃 (L/O) 및 권역별 판권협상을 통해 빠른 시간내에 글로벌 신약으로 자리매김할 수 있을 것이다.” 라는 기대를 밝혔다.
뉴스타운
뉴스타운TV 구독 및 시청료 후원하기
뉴스타운TV
























![[단독] 북한산 인수봉, 구조 헬기 긴급 출동 장면 포착!](/news/photo/202511/669971_628773_447.jpg)






