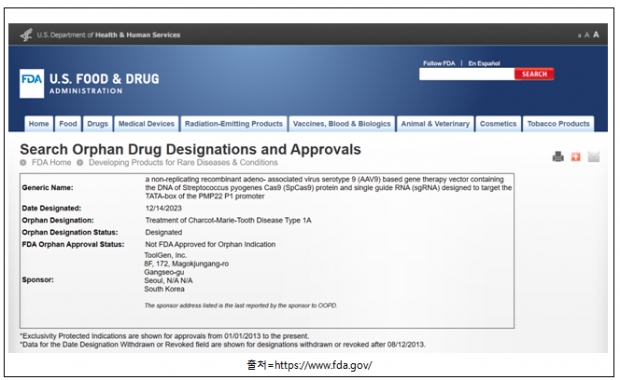
툴젠(대표 이병화) 은 지난 9월 21일 미국 식품의약국(FDA)에 제출했던 말초신경 관련 유전질병인 CMT1A에 대한 유전자 교정 치료제(TGT-001)의 희귀의약품 지정 (Orphan Drug Designation, ODD) 신청이 12월 14일 승인되었다고 밝혔다.
미국 FDA의 희귀의약품 지정은 환자 수 20만명 이하의 희귀난치성 질환 치료제의 개발 및 신속 허가를 지원하는 제도로, 지정되면 임상비용에 대한 세액 공제, 신약 허가 심사비용 면제, 허가 취득 후 7년간의 시장 독점권 등의 혜택이 주어진다.
샤르코-마리-투스병(CMT)은 유전성 말초신경질환으로 근위축, 근력약화, 감각소실, 보행장애 및 무반사 등의 증상을 보이며 전체 CMT 환자의 약 40%가 PMP22 유전자의 중복에 기인하는 CMT1A형 인데, 아직 근본적인 치료법이 없기 때문에 의료적 미충족수요가 높은 상황이다.
툴젠의 유전자 교정 치료제인 TGT-001은 PMP22 유전 서열의 중복으로 인해 단백질이 과발현됨으로 나타나는 말초 신경질환인 CMT1A를 CRISPR-Cas9 system을 통해 과발현된 PMP22의 발현을 정상수준으로 조절하는 기술을 바탕으로 CMT1A의 근본 원인을 교정하여 완치를 목표로 하고 있으며, 현재 동물 실험을 통해 치료 전략에 대한 검증은 마친 상황이다.
㈜툴젠 임상허가제조실장 김소한 상무는 “통상ODD의 신청부터 승인까지의 기간은 90일의 검토기간을 거치는데 툴젠이 최초 FDA에 제출한 신청 서류에 대해 보완의견 없이 승인 처리 되어 예상 회신 기한보다 일주일 가량 일찍 승인 되었다”며, “현재 TGT-001임상시험 준비를 위해 글로벌 최고 수준의 의약품위탁개발생산업체 (CDMO)와 계약을 준비하고 있고, 임상시험 상세 디자인을 수립 중이다”고 말했다.
㈜툴젠 이병화 대표이사는 “이번 FDA 희귀 의약품 지정 신청 승인은 TGT-001의 글로벌 임상 시험 및 사업화를 위한 첫 단계를 성공적으로 완료하였다는데 의미가 있으며, CMT1A질환으로 고통받는 환우분들께 최적의 치료 옵션을 제공하기 위해 더욱 최선을 다하겠다”고 말했다.
뉴스타운
뉴스타운TV 구독 및 시청료 후원하기
뉴스타운TV

























![[특별대담] 제22대 국회의원 선거 자유민주당 인천 서구병 이진기 예비후보](/news/photo/202403/600022_545770_3853.jpg)






![[긴급시국분석] 북한의 내년 4월 총선 전후 기습남침과 좌파들의 내란 및 전민봉기 철저히 대비하라!](/news/thumbnail/202312/592978_536686_4219_v150.jpg)