크리스탈지노믹스가 미국에서 진행중인 슈퍼박테리아 박멸 항생제(개발코드명 CG400549)의 임상2상 전기 시험의 환자 첫 투약이 이미 지난 주에 시작되었다고 19일 전했다.
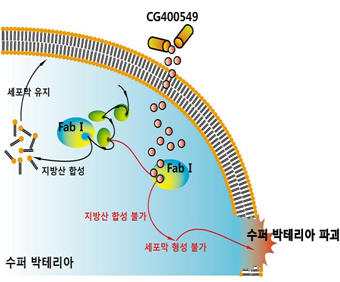
크리스탈지노믹스가 진행 중인 임상2상 전기 시험은 미국 캘리포니아주에서 MRSA(메티실린 내성 황색포도상구균)에 감염된 환자들을 대상으로 진행 중이며 항생제 신약후보의 약효와 안전성을 확인하는 것이 주목적이다. MRSA는 현재 가장 대표적인 슈퍼박테리아중의 하나로 미국에서만 연간 MRSA균에 감염된 환자가 10만 명 정도 발생하고 있고, 이중 약 1만8천 명이 사망할 정도로 치사율이 매우 높은 슈퍼박테리아로 알려져 있다.
현재 전세계 슈퍼박테리아 항생제 시장은 반코마이신(Vancomycin), 뎁토마이신(Daptomycin) 및 자이복스(Zyvox) 등이 주도하고 있으나, 이들에 내성을 지닌 새로운 슈퍼박테리아의 등장으로 치료 효능에 제한이 생기고 있어 새로운 계열의 항생제 신약이 절실히 요구 되고 있는 현실이다. 국제적인 전문 기관인 IMS Health 보고서에 따르면, 화이자의 자이복스(Zyvox)는 2011년 전세계적으로 약 1조 5천억 원에 이르는 매출실적을 보이고 있다.
크리스탈지노믹스는 슈퍼박테리아 박멸 항생제 외에도 현재 관절염 진통소염제(CG100649), 분자표적 항암제 (CG200745)등의 신약후보를 임상개발 중에 있으며, 보건복지부에서 진행한 혁신형 제약기업으로 18일 선정되었다
뉴스타운
뉴스타운TV 구독 및 시청료 후원하기
뉴스타운TV


























![[특별대담] 제22대 국회의원 선거 자유민주당 인천 서구병 이진기 예비후보](/news/photo/202403/600022_545770_3853.jpg)






![[긴급시국분석] 북한의 내년 4월 총선 전후 기습남침과 좌파들의 내란 및 전민봉기 철저히 대비하라!](/news/thumbnail/202312/592978_536686_4219_v150.jpg)